PF Moduł 10: Różnice pomiędzy wersjami
Z Studia Informatyczne
Przejdź do nawigacjiPrzejdź do wyszukiwania
Nie podano opisu zmian |
Nie podano opisu zmian |
||
| Linia 125: | Linia 125: | ||
{| border="0" cellpadding="4" width="100%" | {| border="0" cellpadding="4" width="100%" | ||
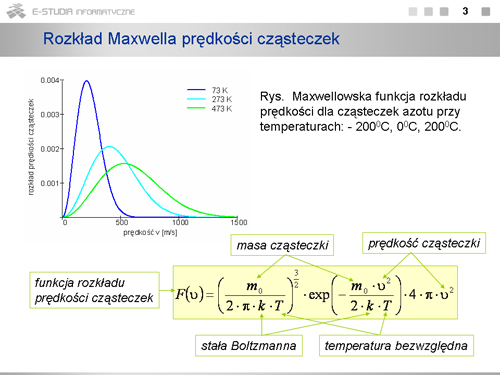
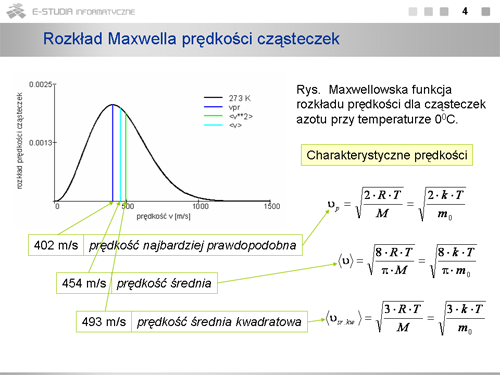
|width="450px" valign="top"|[[Grafika:PF_M10_Slajd8.png]][[Grafika:PF_M10_Slajd9.png]] | |width="450px" valign="top"|[[Grafika:PF_M10_Slajd8.png]][[Grafika:PF_M10_Slajd9.png]] | ||
|valign="top"|Stan układu określany przez parametry makroskopowe, jak temperatura, ciśnienie, energia wewnętrzna, itd. nazywamy makrostanem. Stan układu wyznaczony przez określenie stanów wszystkich cząsteczek wchodzących w jego skład nazywamy '''''mikrostanem'''''. Liczba możliwych mikrostanów odpowiadających danemu makrostanowi jest na ogół ogromna, analiza nasza będzie mieć charakter statystyczny. Liczba mikrostanów odpowiadających danemu makrostanowi nazywa się '''''prawdopodobieństwem termodynamicznym''''' lub '''''wagą statystyczną''''' makrostanu. | |valign="top"|Stan układu określany przez parametry makroskopowe, jak temperatura, ciśnienie, energia wewnętrzna, itd. nazywamy '''''makrostanem'''''. Stan układu wyznaczony przez określenie stanów wszystkich cząsteczek wchodzących w jego skład nazywamy '''''mikrostanem'''''. Liczba możliwych mikrostanów odpowiadających danemu makrostanowi jest na ogół ogromna, analiza nasza będzie mieć charakter statystyczny. Liczba mikrostanów odpowiadających danemu makrostanowi nazywa się '''''prawdopodobieństwem termodynamicznym''''' lub '''''wagą statystyczną''''' makrostanu. | ||
Rozpatrzmy sens wagi statystycznej na przykładzie naczynia z gazem, w którym znajduje się <math>N\,</math> cząsteczek. Stan danej cząsteczki opiszemy tylko jedną informacją - w której części naczynia, lewej czy prawej, cząsteczka się znajduje. Zbiór tych informacji dla wszystkich <math>N\,</math> cząsteczek określa '''mikrostan''' naszego układu. (Dla uproszczenia rozważań nie będziemy brać pod uwagę prędkości, kierunku ruchu, masy cząsteczek itp.). | Rozpatrzmy sens wagi statystycznej na przykładzie naczynia z gazem, w którym znajduje się <math>N\,</math> cząsteczek. Stan danej cząsteczki opiszemy tylko jedną informacją - w której części naczynia, lewej czy prawej, cząsteczka się znajduje. Zbiór tych informacji dla wszystkich <math>N\,</math> cząsteczek określa '''mikrostan''' naszego układu. (Dla uproszczenia rozważań nie będziemy brać pod uwagę prędkości, kierunku ruchu, masy cząsteczek itp.). | ||