PF Moduł 8: Różnice pomiędzy wersjami
Z Studia Informatyczne
Przejdź do nawigacjiPrzejdź do wyszukiwania
Nie podano opisu zmian |
Nie podano opisu zmian |
||
| Linia 95: | Linia 95: | ||
{| border="0" cellpadding="4" width="100%" | {| border="0" cellpadding="4" width="100%" | ||
|valign="top" width="450px"|[[Grafika:PF_M8_Slajd7.png]] | |valign="top" width="450px"|[[Grafika:PF_M8_Slajd7.png]] | ||
|valign="top"| | |valign="top"|Jeśli proces zachodzi pod stałym ciśnieniem, czyli <math>p=const</math>, to mówimy, że zachodzi '''przemiana izobaryczna'''. Z równania stanu wynika, że w tym przypadku objętość jest liniową funkcją temperatury. Przy wzroście objętości praca jest wykonywana przez gaz <math>(W<0, W'>0)</math>, a przy zmniejszeniu objętości, przez otoczenie, <math>(W>0, W'<0)</math> Ciśnienie zachowuje stałą wartość, więc '''praca''' wykonana nad układem w przemianie izobarycznej wynosi | ||
: <math>W=-\int_{V_1}^{V_2} p \cdot dV=-p \cdot \int_{V_1}^{V_2} dV=p \cdot (V_1-V_2)</math>. | |||
Podwyższenie temperatury o jeden kelwin wymaga więcej ciepła niż w przypadku ogrzewania bez zmiany objętości, bowiem część ciepła zużywana jest na wykonanie pracy. | |||
W procesie izobarycznym energię wewnętrzną możemy zmienić zarówno na drodze wykonania pracy jak i wymiany ciepła | |||
: <math>dU=\delta Q_p-p \cdot dV</math>. | |||
Wyrażenie to możemy przepisać dla <math>n_M</math> moli w innej postaci wykorzystując poznane wzory: | |||
: <math>n_M \cdot C_v \cdot dT=n_M \cdot C_p \cdot dT - p \cdot dV</math> | |||
gdzie wprowadziliśmy pojęcie '''ciepła molowego przy stałym ciśnieniu''' | |||
: <math>C_p={\delta Q_p \over dT}</math>. | |||
Różniczkując równanie stanu dla procesu izobarycznego, w którym <math>p=const</math> mamy | |||
: <math>p \cdot dV=n_M \cdot R \cdot dT</math> | |||
Wykorzystując ten związek możemy napisać, że | |||
: <math>n_M \cdot C_v \cdot dT = n_M \cdot C_p \cdot dT - n_M \cdot R \cdot dT</math> | |||
skąd otrzymujemy równanie Mayera | |||
: <math>C_p=C_v+R</math>. | |||
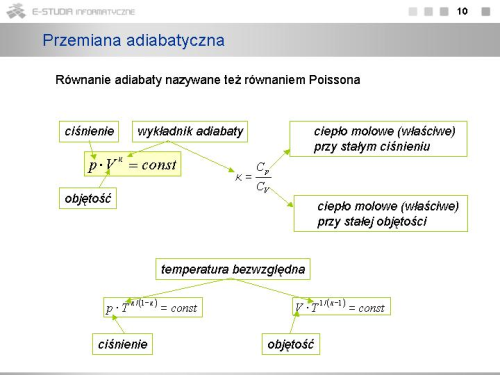
Stosunek ciepła właściwego przy stałym ciśnieniu do ciepła właściwego przy stałej objętości jest parametrem określającym rodzaj gazu i oznaczany jest zwykle symbolem <math>\kappa</math> (kappa). | |||
: <math>\kappa = {C_p \over C_v}</math>. | |||
Wykorzystując równanie Mayera można ciepła molowe <math>C_p</math> i <math>C_v</math> wyrazić za pomocą współczynnika <math>\kappa</math>. | |||
: <math>\kappa = {C_v + R \over C_v}=1+{R \over C_v}</math> lub <math>C_v={R \over \kappa-1}</math>, <math>C_p={\kappa \cdot R \over \kappa - 1}</math>. | |||
Ze związków tych widzimy, że <math>\kappa > 1</math>. | |||
|} | |} | ||
Wersja z 12:30, 23 sie 2006

|
Wprowadzenie
Omówione są tu ogólne prawa makroskopowe opisujące prawidłowo zjawiska cieplne i pozwalające ilościowo przewidywać skutki różnych procesów. |

|

|
|